ScienceBits
Lente Gábor blogja
Az LIII. Irinyi János Középiskolai Kémiaverseny egyik feladattípusának megoldásához
KÖZÉPISKOLAI KÉMIAI LAPOK
2020 szeptemberétől lépett életbe az új Nemzeti Alaptanterv, amelyben a kémiára szánt óraszám sajnálatosan – de a súlyos szaktanárhiányt látva korántsem érthetetlenül – lecsökkent. Az Irinyi János Országos Középiskolai Kémiaverseny régóta követett alapelve, hogy az ott szereplő feladatok megoldásához nem szükséges annál több kémiai ismeret, mint amennyit a szokásos középiskolai tanmenetek előírnak. Az óraszámcsökkenéssel együtt természetesen csökkent a tananyag mennyisége is, illetve versenyszervezési szempontból további, már a 2020/21-es tanévben a kilencedik osztályosok között is jól érzékelhető nehézséget jelent az, hogy a korábbi kategória-besorolási rendszer is idejét múlttá vált: az egyes középiskolákban ténylegesen kémiára fordított óraszám a korábbinál sokkal változatosabbá vált.
Természetesen ezeket a változásokat a versenyen kitűzött feladatokban sem lehetett figyelmen kívül hagyni. A versenykiírásban szereplő témaköröket a versenybizottság már 2020 őszén hozzáigazította a megújult Nemzeti Alaptantervhez. Ebből következően a korábbinál szűkebb kémiai ismeretek feltételezésével kell(ene) olyan feladatokat írni, amelyek egyrészt alkalmasak arra, hogy a legtehetségesebbeket kiválasszák a versenyzők közül, de ugyanakkor nem nehezek annyira, hogy sok diák kedvét elvegyék a versenyen való megmérettetéstől. A középiskolai kémiai tanulmányi versenyeken szereplő feladatok jelentős része olyan, viszonylag korlátozott számú sémák egyikét követi, amelyet egy tapasztalt felkészítő tanár a szöveg elolvasásával egy időben felismer.
2020-ban jelent meg a jelen cikk egyik szerzőjének Ezeregynél is több molekula meséi című műve. A könyv arra tesz tudatos kísérletet, hogy a kémia összetett jelrendszerének (így például kémiai képleteknek) a használata nélkül, kizárólag nyelvi eszközökkel ismertesse meg az olvasóval a kémiatudomány alapösszefüggéseit, illetve a vegyészek gondolkodásmódját. A különböző anyagok elnevezéséről szóló fejezet egyik bekezdése a következőképpen próbálja meg érzékeltetni azt, hogy miért is célszerű dolog szerkezeti képleteket használni:
„Már többször szó esett az … nevű anyagról. Kémiai képletet továbbra sem írok le, de azt azért megosztom az olvasóval, hogy ez a név a szakemberek számára sok információt tartalmaz. Van benne egy négy szénatomot és egy oxigénatomot tartalmazó ötszög. Ebben az oxigénatom melletti szénatomhoz egyetlen oxigén kapcsolódik, és semmi más; az oxigénnel nem szomszédos szénatomok mindegyikéhez egy oxigénatom kapcsolódik, ahhoz pedig még egy hidrogénatom úgy, hogy a hidrogének a szénhez már nem kapcsolódnak. A gyűrűben lévő utolsó, ismét oxigén melletti szénatomhoz egy hidrogénatom és egy két szénatomból álló, kis lánc kapcsolódik; a kis lánc mindegyik szénatomjához egy oxigénatom, majd ehhez egy hidrogénatom is kötődik. A kis lánc gyűrű melletti szénatomjához egy, a gyűrűtől távolabbihoz két további hidrogén kötődik. Emellett a név még azt is megmondja, hogy a kis láncban lévő, a gyűrűhöz közvetlenül kapcsolódó szénatom, illetve a gyűrűben lévő, közvetlenül a kis lánchoz is kapcsolódó szénatom körül milyen térbeli elrendeződésben kapcsolódik az a négy atom, amely kötődik hozzá. (Ezt már nincs kedvem ennél pontosabban kifejteni.)”
Az eredeti szövegben a … helyén egy nagyon gyakori vegyület kémikusok számára is meglehetősen idegenül hangzó szabályos neve szerepel. A vegyület neve és képlete a jelen cikk végén megtalálható. Arra bátorítjuk az olvasót, hogy mielőtt odalapozna, próbálja meg a leírás alapján a szerkezeti képletet felírni.
Az Irinyi-verseny II. kategóriájában tizedik osztályosok indulnak, ők ebben az évben szerves kémiát tanulnak. Lényegében az idézett könyvbekezdés adta az ötletet, hogy versenyfeladatot is lehetne úgy készíteni, hogy a szövegben felsoroljuk egy molekula néhány szerkezeti jellemzőjét, amely már elégséges az azonosításhoz. A versenykiírás témakörei között a II. kategória első fordulójáig csak a szénhidrogének szerepelnek, így a feladat (a megoldással együtt) a következő lett:
Első forduló, II. kategória
E2. feladat (14 pont)
A megadott információk alapján azonosítsd, melyik szénhidrogénről van szó! Add meg a szerkezeti- és az összegképletét!
| A szénhidrogén szerkezeti- és összegképlete: | |
| a) Benne a hidrogénatomok száma háromszorosa a szénatomok számának. |
C2H6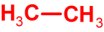 |
| b) Az összes benne lévő kötés energiája azonos. |
CH4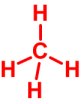 |
| c) A legkisebb sűrűségű, két szénatomot tartalmazó szénhidrogén. |
C2H2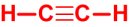 |
| d) A leghosszabb szénlánc négy szénatomot tartalmaz, és van benne tercier és kvaterner szénatom is. |
C7H16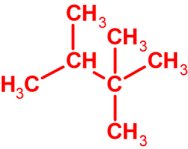 |
| e) Egyetlen gyűrű van benne, az hat szénatomot tartalmaz, nincsen benne primer szénatom, a hidrogének száma a szénatomok számának kétszeresénél kettővel kevesebb. |
C6H10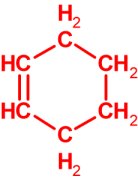 |
| f) Hat atomot tartalmaz, mindegyik egy egyenesen van. |
C4H2 |
| g) A legkisebb olyan telített szénhidrogén, amelyben az összes szénatom tercier. |
C4H4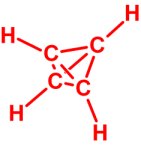 |
Talán nem túlzás azt állítani, hogy a feladat látszólagos egyszerűsége ellenére elég változatos logikai okfejtéseket kell használni ahhoz, hogy eljussunk a végeredményre. Az a) részben például azt kell észrevenni, hogy a CH3 tapasztalati képletnek csak egyetlen egy stabil szerves molekula felel meg. A b) részben az a fő felismerés, hogy ha egy szénhidrogénben csak egyetlen típusú kötés van, akkor annak szén-hidrogén kötésnek kell lennie. A c) rész megoldásához a gázok molekulatömege és sűrűsége közötti összefüggés ismerete alapján kell azt a molekulát megkeresni, amelyben két szénatom mellett a lehető legkevesebb hidrogén van. Ezen feladatoknak fontos részfelismerése az is, hogy a logikailag megállapítható molekulaképlethez csak egyetlen szerkezeti képlet tartozhat, mert az atomok kapcsolódási sorrendjére vonatkozó információt egyik meghatározás sem ad.
Más a helyzet a maradék négy példában: itt a szöveges definíció már a szerkezetre utaló információt is tartalmaz. A d) rész leginkább a rendűség fogalmának pontos értelmezésén alapul, míg az e) részben is szükség van erre annak megállapításához, hogy a gyűrűhöz nem kapcsolódhat oldallánc, vagyis a gyűrűnek kell hattagúnak lennie. Az f) résznél a szokásos kötésszögek, illetve molekulageometriák ismerete alapvető fontosságú, míg a g) résznél az jelent plusz nehézséget, hogy itt a megoldást már semmiképpen nem lehet a szerkezeti képleteknél amúgy nagyon is szokásos módon, síkban kiterítve elképzelni (még a szénvázát sem!)
Ahogy említettük, az Irinyi-verseny feladatainak írásánál arra kell törekedni, hogy egyrészt eléggé nehezek legyenek ahhoz, hogy csak az indulók nem túl nagy hányada érjen el maximálishoz közeli eredményt, másrészt viszont olyan résztvevő lehetőleg egy se legyen, akinek csak kudarcélményt jelent a verseny. A most bemutatott feladattípus igen jól alkalmazkodik ehhez a követelményhez, mert lehetővé teszi a fokozatosan nehezedő meghatározások írását. Természetesen ilyenkor a legkönnyebb kérdéssel kell kezdeni a feladatot, márcsak azért is, hogy a megoldók ne adják fel a feladat szövegének olvasását az első mondatok után. Az is nagyon fontos, hogy egy-egy példa nehézségét ne kizárólag a szerző ítélje meg. Ezért a feladatsorok, illetve az egyes feladatok is többlépcsős finomításon mennek át, mielőtt elnyerik végleges formájukat. Az itt elvégzett változtatások az apróbb, megfogalmazásbeli pontosítástól egészen a feladat teljes kihagyásáig terjedhetnek. Az előbb bemutatott, első fordulós feladatból például az érlelési folyamat eredményeképp a következő két kérdést tejesen elhagytuk:
| h) A vegyületben minden szénatom gyűrűben van, tartalmaz két teljes benzolgyűrűt, amelyek egy orto-helyzetű metiléncsoport-páron keresztül kapcsolódnak. |
C14H12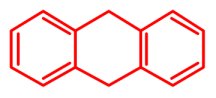 |
| i) A vegyületben minden szénatom gyűrűben van, tartalmaz két teljes benzolgyűrűt, amelyek két, az egyik gyűrűn para-, a másikon meta-helyzetű, két metiléncsoportból álló láncon keresztül kapcsolódnak. |
C16H16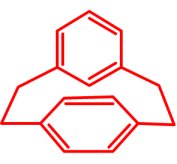 |
Rutinos tanárkollégáink mindkét esetben az orto, meta, para szerkezeti nevezéktan használatáról gondolták azt, hogy meghaladja a versenyen indulók túlnyomó többségének előismereteit, illetve az i) pontban nagyon is szükséges (habár a „kivasalva” felrajzolt szerkezeti képletből egyáltalán nem nyilvánvaló) térbeli gondolkodás nehézségei miatt nem tartották alkalmasnak a feladatrészt az első fordulóba.
A második forduló témakörei a versenykiírás szerint a halogén- és oxigéntartalmú szerves anyagokkal bővülnek, az utóbbiak közül elsősorban az alkoholokra és ketonokra koncentrálva. A vegyület-leírásos feladat alkalmasnak bizonyult arra is, hogy az Irinyi-versenybizottság zsargonjában „futó feladat”-ként emlegetett sorozat legyen belőle, vagyis azonos alapgondolatra építve egy nehezebb, bővített forma a következő fordulóba is bekerült:
Második forduló, II. kategória
E4. feladat (19 pont)
Az alábbi szerves vegyületek csak szenet, hidrogént és oxigént tartalmaznak. A megadott információk alapján azonosítsd, melyik vegyületről van szó! Add meg a szerkezeti- és az összegképletét!
| A csak oxigént, szenet és hidrogént tartalmazó szerves vegyület szerkezeti- és összegképlete: | |
| a) Alkohol, amelyben egyetlen oxigén van és nincs szén-szén kötés. |
CH4O |
| b) A legkisebb szénatomszámú, nyílt láncú, telített, szekunder alkohol. |
C3H8O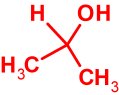 |
| c) A legkisebb moláris tömegű, csak szén–hidrogén és szén–oxigén egyszeres kötéseket tartalmazó molekula. | C2H6O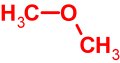 |
| d) A legkisebb molekula, ahol a hidrogének száma megegyezik a szénatomok és oxigénatomok számának összegével. |
CH2O |
| e) A legkisebb molekula, ahol a hidrogénatomok száma kétszer annyi, mint a szénatomok és oxigénatomok számának összege. |
CH4O |
| f) Hidrogént nem tartalmazó lineáris molekula, amelyben öt atom van. |
C3O2 |
| g) Huszonegy atomból álló molekula, amiben a hidrogén-atomok száma a szénatomok számának kétszerese, ami az oxigénatomok számának a kétszerese. Minden szénatomja egyenértékű, minden oxigénje egyenértékű, valamint minden hidrogénje egyenértékű. (Ez a vegyület egyébként a korona-éterek csoportjába tartozik.) |
C6H12O3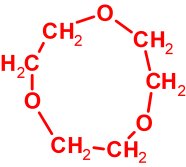 |
| h) Négy darab, 1,3-helyzetű éterkötéseken át kapcsolódó benzolgyűrűből álló molekula. Atomjai számának az összege 44. |
C24H16O4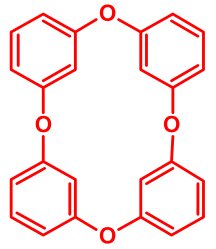 |
A halogének lehetséges jelenléte nem igazán növelte az elkészíthető feladatok változatosságát, hiszen szerkezeti szempontból egy halogén semmivel nem tud többet, mint egy hidrogén. Az oxigénnel azonban már más a helyzet: ez minőségi változást jelentett. Ezért a második fordulóban nem kettő, hanem öt meghatározásnál volt a megoldás egyik célravezető útja az, hogy a leírt szöveg alapján meghatározzuk a molekulaképletet, majd megkeressük hozzá az egyetlen lehetséges szerkezeti képletet. A feladatszerző egy pici mókát is megengedett magának: a metanolt két különböző módon is definiálta.
Az f) részről könnyen felismerhető, hogy az első fordulós feladat f) részével rokon: itt is az egymáshoz lineáris láncban kapcsolódó (tehát egyetemen sp hibridizációjúnak nevezett) szénlánc megfelelő lezárását kellett megtalálni.
A g) rész azonban már komoly újdonság az előző fordulóhoz képest: itt a megadott szöveg alapján a C6H12O3 molekulaképletig viszonylag könnyű eljutni, de ehhez számolatlanul lehet szerkezeti képleteket alkotni; az Amerikai Kémiai Társaság SciFinder adatbázisa például e sorok írásának idején 1717 darab különböző, már a valóságban is előállított izomert tartott nyilván.
Ezt az alkalmat megragadva szeretnénk leírni a szerves anyagoknál a molekulaképlet és a szerkezeti képlet közötti összefüggés keresésének egy olyan módszerét, amelyet a legtöbb, ilyen problémákban járatos kémikus használ (akár tudatosan, akár ösztönösen):
- A kiindulási pont mindig a telített, gyűrűt nem tartalmazó szénhidrogén CnH2n+2 összegképlete.
- Oxigénatom hozzáadása nem változtat a telített vegyületben lévő hidrogének számán.
- Egy nitrogénatom hozzáadása eggyel növel a telített vegyületben lévő hidrogének számát.
- Egy halogénatom hozzáadása eggyel csökkenti a telített vegyületben jelen lévő hidrogének számát.
- A telítetetlen vegyületekben a hidrogének száma ennél csak kevesebb lehet: a vegyületben lévő gyűrűk és többszörös kötések összes száma éppen a telített összetételhez képest hiányzó hidrogénatomok számának a fele.
- Kén- és foszforatomot tartalmazó molekulákra sajnos közvetlenül nem, és haladóbb formában is csak eléggé összetett módon alkalmazhatók ezek a szabályok; ezek részletezésétől eltekintünk.
Az 5. szabály alkalmazásánál még érdemes arra emlékezni, hogy egy hármas kötés ilyen szempontból két kettős kötéssel ekvivalens. Megemlítjük még, hogy a szabályt akár pusztán a gyűrűk számával is ki lehet(ne) mondani, hiszen egy kettős kötést geometriai szempontból minden további nélkül el lehet képzelni két szénatomos gyűrűként, egy hármast kötést pedig két azonos szénatom részvételével megalkotott gyűrűpárként.
Egyszerű példaként képzeljük el a CHN összegképletet. Egy szén és egy nitrogénatomhoz a teljesen telített vegyület képlete CH5N lenne, így a CHN-nek (sokkal hagyományosabb, de igazából a szerves kémiai konvencióknak kevésbé megfelelő sorrendben felírva HCN) vagy két kettőskötést kell tartalmaznia, vagy egy hármast, vagy egy kettőskötés és egy gyűrűt, vagy két gyűrűt. Ugyanígy a C30Cl3I2H57O7N2 molekulaképletből is kis számolás után belátható, hogy vagy egyetlen kettőskötés tartalmaz (de ez nemcsak szén-szén kettős kötés, hanem szén-oxigén, szén-nitrogén, vagy kicsit rémképzetszerűen akár még nitrogén-oxigén is lehet), vagy egyetlen gyűrűt.
Ha számolásnál a többszörös kötések és gyűrű teljes számára nem jön ki egész szám (mivel kettővel osztunk, ekkor egy páratlan egész szám fele az eredmény), akkor a szerves kémiában hagyományos vegyértékszemléletben nincs ilyen képletű molekula, mert az elektronok összes száma ilyenkor páratlan lenne, azaz feltétlenül van köztük legalább egy párosítatlan. Ilyen például a C6H5 esete, amelyről a legtöbb olvasó is valószínűleg azonnal meglátja, hogy egy gyök képlete. Néhány kivételes esetben a szerves kémia hosszan eltartható gyököket is ismer, de ezeket stabil gyököknek szokták nevezni, és nem páratlan molekuláknak.
Mindezek ismeretében visszatérve a C6H12O3 molekulaképletű g) feladatrészre: itt a szabályok alkalmazásával azt kapjuk, hogy a szerkezeti képletben vagy egy kettős kötés, vagy egy gyűrű van. A további információ az, hogy a molekula minden szénatomja egyenértékű, minden oxigénje egyenértékű, és minden hidrogénje is egyenértékű. Ez kizárja a kettőskötés lehetőségét, hiszen ekkor a kettőskötéssel összekapcsolt két atom biztosan nem lehetne a többivel egyenértékű, olyan atomfajta pedig nincs a molekulában, amelyből csak kettő darab volna. Azt is lehet látni, hogy ha az összes hidrogén egyenértékű, akkor mindegyiknek azonos típusú atomhoz kell kapcsolódnia, ez pedig csak a szénatom lehet, hiszen oxigénatomból ehhez nincs elég. Így a szénatomok egyenértékűségét is „bevetve” felismerhetjük, hogy a vegyületben hat darab metiléncsoportnak kell lennie, és mivel sem hidrogén-oxigén kötés, sem legfeljebb egy hidrogénhez kapcsolódó szénatom nincsen, ezért mindhárom oxigén éteres formában van. Ha eddig eljut valaki, akkor lényegében megoldotta a feladatot, mert hat metiléncsoportból és három oxigénből csak egyféleképpen lehet molekulát alkotni úgy, hogy az oxigének egyenértékűek legyenek.
A feladat h) része lényegesen könnyebb, mint az őt megelőzők; itt a képlet felírásához elég „receptszerűen” követni a leírásban meglelhető szerkesztési utasítást.
Az itt felsorolt meghatározások közös sajátsága volt, hogy minden esetben egyetlen szerkezeti képlet felelt meg a leírásnak. Természetesen nehezíthető egy ilyen típusú feladat úgy, ha egynél több (de persze azért kevés) megoldás van. Ezzel azonban a feladatszerzőknek is óvatosan kell bánniuk: nagyon természetes emberi hozzáállás az, hogy ha talál valaki egy megoldást, akkor továbbiak keresésével nem tölti az időt. Így ebben az esetben a feladat szövegétől elvárható minimum az, hogy a több lehetséges megoldás lehetőségére felhívja a figyelmet, de az sem túlzás, ha minden egyes meghatározáshoz megadja a keresett megoldások számát. Arra is itt szeretnénk felhívni a figyelmet, hogy ha megoldásként a molekula nevét is meg kell adni, akkor az jelentős mértékben csökkentheti a feladat változatosságát: már az itt felsorolt, az Irinyi-versenyen feladott példák között is van olyan, amelynek szabályos nevének megszerkesztésére ezen cikk írói sem vállalkoznának.
A 2020/21-es tanévben sajnos elmaradt az Irinyi-verseny harmadik fordulója, az országos döntő. Az élet viszont úgy hozta, hogy erre a feladatok előkészítése nagyrész megtörtént. A versenykiírás szerint ekkor már a II. kategória témakörei közé tartoznak az összetett funkciós csoportot tartalmazó oxigén-, valamint nitrogéntartalmú szerves vegyületek (karbonsavak, észterek, aminok, amidok, aminosavak, heteroaromások) is. Ennek figyelembe vételével elkészült a „futó feladat” harmadik fordulós változata is, de ez a diákok kezébe már nem jutott el. Ezek mindegyikét nem szeretnénk itt bemutatni, hiszen nagyon-nagyon reméljük, hogy 2022-ben már lesz döntő és esetleg az ötletek ott hasznosabbak lehetnek, mint amilyenek az idén voltak. Ezért ezekből csak két olyat mutatunk be, amelynek az alapgondolata már az előző két fordulóban is világosan felismerhető, és amelyeknél a molekulaképlet megfejtése magától értetődő, a szerkezet azonban nem:
| 1-1-1 szén, oxigén- és nitrogénatomot és 3 hidrogénatomot tartalmazó, síkalkatú molekula: |
CH3NO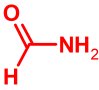 |
| Két szén- és két nitrogénatomból álló, lineáris molekula: |
C2N2 |
Végezetül pedig a cikk elején, a negyedik bekezdésben körülírt szerkezeti képletet mutatjuk be jutalmul azon olvasóknak, akiknek türelme mindeddig kitartott:
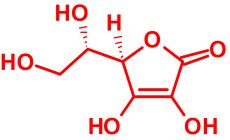 |
A … helyén az eredeti könyvben a szabályos név szerepel, vagyis (R)-3,4-dihidroxi-5-[(S)-1,2-dihidroxietil]furán-2(5H)-on, de az emberek többsége ezt az anyagot inkább aszkorbinsav vagy C-vitamin néven ismeri.
Az Irinyi-verseny első és második fordulójának feladatsorai, illetve részletes javítási útmutatója az alább URL-ekről tölthetők le:
![]() 2021.05.20.
2021.05.20.
