ScienceBits
Lente Gábor blogja
Űrszondabaleset a Titán egyik metántavában
KÖZÉPISKOLAI KÉMIAI LAPOK, SZAKMAI
Készült a Kozmikus Baleseteket Kivizsgáló Intézet (KOBALKIVI) 2222. február 22-én kiadott jelentése alapján

1. Háttérinformáció
1.1. A Titán
A Titán a Szaturnusz legnagyobb holdja, a Cassini űrszonda által 2005-ben készített fényképe az 1. ábrán látható. A földlakók számára létezését Christiaan Huygens (1629-1695) holland tudós fedezte fel 1655. március 25-én. A Föld felszínéről szabad szemmel nem, de már kis távcsővel is látható a Szaturnusz mellett, helyét naponta változtató fénypontként. Átmérője 5150 km (a Föld átmérőjének 40%-a), tömege 1,3∙1023 kg (a Föld tömegének 2%-a), a Szaturnusztól mért átlagos távolsága 1,2 millió km, Szaturnusz körüli keringési ideje pedig 382 óra. A Naprendszer második legnagyobb méretű holdja, egyedül a Jupiter körül keringő Ganümédesz nagyobb nála.
A XX. században fedezték fel, hogy a Titánon nagy mennyiségű szénhidrogén, főleg metán és etán található. A Titán hőmérsékleti és nyomásviszonyai alapján már ekkor is sejtették, hogy ezek jelentős része folyékony halmazállapotban lehet jelen a felszínen. 2010-ben végzett radarmérések arra utaltak, hogy a szénhidrogénekből álló tavak az évszakoktól függően elpárologhatnak és újra lecsapódhatnak, így a Titán féltekéi között látszólagos vándorlást végeznek. Ugyanezen mérések azt mutatták, hogy az egyik legnagyobb metántó, amelynek neve Ontario, nagyon sekély: átlagos mélysége 0,4-3,2 m, legmélyebb pontja pedig mindössze 2,9-7,4 m lehet. Így a tó sokkal nagyobb területű, s ugyanakkor sekélyebb, mint a Balaton. Az északi féltekén található Ligeia nevű tó mélyebb volt, mint a radarral maximálisan mérhető 8 m.
A Titán az egyetlen hold a Naprendszerben, amelynek jelentős légköre van; ez főként nitrogénből áll, kisebb mennyiségben pedig szénhidrogéneket, elsősorban metánt tartalmaz. Folyékony víz egyensúlyban semmilyen nyomáson nem létezhet -22 °C-nál alacsonyabb hőmérsékleten. Erről a víz fázisdiagramja tanúskodik, amely a Középiskolai Kémiai Lapok 2008. évi 1. számában publikált, Jég-kilenc a Macskabölcsőben című írásban is megtalálható. Folyékony víz így a Titánon sem lehet, mert a hőmérséklet rajta mindig jóval kisebb 22 °C-nál, de szilárdan, jég formájában a hold kőzeteinek egyik fő alkotóanyaga. A nagyon alacsony hőmérséklet miatt a légkörben is csak igen csekély mennyiségű víz lehet.
1.2. A Titán szirénjei
Már a XXI. század elején gondoltak arra, hogy a Titán felszínén lévő metántavakban – a Föld tengereihez hasonlóan – létezhetnek élő szervezetek. Az ilyen élőlények oxigén helyett hidrogént lélegeznének be, glükóz helyett acetilént használnának energiaforrásként, s szén-dioxid helyett metánt lélegeznének ki. (A szén-dioxid a Titán felszínén uralkodó körülmények között egyébként is szilárd anyag.) A Földön is ismeretesek úgynevezett metanogén baktériumok, amelyek ugyan vízben élnek, de folyékony metánban a bennük lévő szerves molekulákat nem kellene a hidrolízistől védeni. 2010-ben megállapították, hogy a Titán légkörének magasabb régióiban sokkal több hidrogén van, mint a felszín közelében; ebből az is következhet, hogy a felszínen valamilyen folyamatok elfogyasztják a hidrogént. Hasonlóképpen az acetilén koncentrációját is váratlanul kicsinek mérték a felszínen. Azonban az még nyitott kérdés, hogy az acetilén és a hidrogén reakcióját milyen anyaggal lehet katalizálni 95 K körüli hőmérsékleten.
A Titánon élő intelligens lényekkel a XXIII. század első évtizedében sikerült kapcsolatot teremteni. Kurt Vonnegut (1922-2007) amerikai író 1959-ben kiadott regényének címét követve a lények elterjedt neve a „Titán szirénjei” lett. A velük való kapcsolat kizárólag rádiókommunikációra korlátozódik, testük felépítéséről vagy biokémiájáról semmilyen adat nincsen. A Szaturnusz körül keringő emberi űrszondák megfigyelései alapján biztosra vehető, hogy 2211-ben a Mimasz megabaktériumainak invázióját a Titán lényei elemi erővel verték vissza. A hódító flotta megmaradt űrhajóinak a javítását emberi támaszpontokon végezték, és a rajtuk található sérülésnyomok alapján legalább négy különböző típusú fegyver használatára lehetett következtetni, amelyek közül a kaontorpedónak elnevezett robbanó eszköz volt a leghatásosabb. Politikai elemzők ezen háború és a Titán szirénjeivel folytatott, egyébként nem ellenséges üzenetváltások alapján biztosra veszik, hogy a lények tisztában vannak azzal, hogy a holdjuk feszínén lévő szénhidrogén-készletek igen értékesek az emberiség számára, és akár fegyveres konfliktus vállalása árán is készek távoltartani minden nem kívánatos beavatkozást.
2. A baleset
A Szaturnusz-Titán-Rádiószonda (SzaTiR-112358) 2221. június 22-én sikeresen leszállt a Titán felszínére. Elsődleges feladata tudományos megfigyelés volt ugyan, de politikai elemzők már a küldetés tervezésekor figyelmeztettek arra, hogy a Titán szirénjei a leszállást minden bizonnyal újabb hódítási kísérletnek tartják majd. A szonda a biztonságos landolást megerősítő jelzések leadása után még 5 perc 28 másodpercig a terveknek megfelelően működött, majd hirtelen beszüntette rádióadását. Röviddel ez után a Titán szirénjei rádióüzenetben tudatták, hogy a szonda egy folyékony metánnal teli tóban úszva jéghegynek ütközött és működésképtelenné vált. A szondával történtek tisztázására az egyetlen lehetőség a helyszínen történő személyes vizsgálat volt.
3. Pirx kapitány jelentésének kivonata
Pirx kapitány akkor még csak elképzelt kalandjairól Stanislaw Lem (1921-2006) lengyel író 1966 és 1968 között írta azon műveit, amelyek a XX. század végére kötelező olvasmányok lettek Lengyelország középiskoláiban. A valódi Pirx kapitány a baleset idején űrhajójával és tizennyolc főnyi legénységgel éppen a Neptunusz felé repült kereskedelmi céllal. Parancsot kapott a haladéktalan pályamódosításra és a szonda megkeresésére a Titánon. Egyúttal felhívták a figyelmét, hogy szigorúan kerüljön minden olyan tevékenységet, amelyet a Titán szirénjei ellenségesnek tarthatnak.
Pirx kapitány bonyolult és kellően előkészítetlen, de végül is sikeres űrmanőverek sorozata után 2221. december 24-én pályára állt a Titán körül. Űrhajója távérzékelők segítségével a tervezett leszállási hely közvetlen közelében hamarosan meg is találta az űrszonda maradványait. Ezután egyszemélyes űrkabinjában leszállt a felszínre a szonda mellett. Felszerelésében tudományos eszközök alig voltak, ezért csak a hőmérsékletet (128 K) és a légnyomást (154 kPa) tudta megmérni. Leírásában a szonda megtalálási helyét a Marson lévő kiszáradt tóvidékhez hasonlította, a környéken ugyanakkor nem találta tényleges tavak nyomát. A sérült űrszondát űrkabinjában visszavitte az űrhajó fedélzetére. Az egyetlen értelmes adat, amit technikusának sikerült kinyernie a szonda memóriájából, a közvetlenül a leszállás után rögzített környezeti hőmérséklet (94 K) és nyomás (142 kPa) volt. A legénység egyik tagja korábban részt vett a mimaszi megabaktériumok flottájának szervizelésében, ő a szonda sérüléseit egy kaontorpedó becsapódásának tulajdonította. A szonda megtalálási helyétől távol, a Titán téli oldalán metántavakat azonosítottak. Pirx kapitány néhány nappal később már folytatta is útját eredeti úticélja felé.
4. Kísérleti leírás
Noha a metán tulajdonságai jól ismertek a szakirodalomból, a KOBALKIVI vezetői arra a belátásra jutottak, hogy ilyen súlyú politikai következményekkel járó tudományos kérdésben csak közvetlen kísérleti adatok alapján mondhatnak megalapozott véleményt. Az első kísérletsorban speciálisan kiképzett, zárt tartályban melegítettek 64,0 g tiszta metánt, s közben nagy pontossággal mérték a nyomást. A tartály teljes térfogata 2800 cm3 volt, s nem változott a melegítés hatására. A kiindulási hőmérsékletet 80,00 K, a fűtési sebesség 10,0 J/s-os, állandó érték volt. A melegítés közben regisztrált adatok a következők:
| t (s) | 0 | 100 | 200 | 207 | 350 | 578 | 700 | 1000 | 2000 | 3000 | 4000 | 5000 | 5212 | 5250 | 5300 |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| T (K) | 80,00 | 85,41 | 90,32 | 90,67 | 90,67 | 90,67 | 95,26 | 105,17 | 127,77 | 142,53 | 153,44 | 161,68 | 164,40 | 167,51 | 171,31 |
| p (Pa) | 2615 | 5922 | 11420 | 11702 | 11702 | 11702 | 20641 | 57186 | 322674 | 742101 | 1238641 | 1741874 | 1949783 | 1986668 | 2031736 |
Egy másik sorozatban ugyanezt az eszköz használva megismételték a kísérletet úgy, hogy 64,0 g metán mellé még 1,471 g héliumot is a tartályba zártak. Az adatok:
| t (s) | 0 | 100 | 200 | 213 | 300 | 585 | 714 | 1214 | 2214 | 3214 | 4214 | 5214 | 5504 | 5514 | 5614 |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| T (K) | 80,00 | 85,29 | 90,10 | 90,74 | 90,74 | 90,74 | 95,49 | 110,74 | 131,00 | 144,78 | 155,10 | 162,89 | 166,30 | 167,20 | 174,54 |
| p (Pa) | 93865 | 103092 | 113840 | 115162 | 115757 | 116242 | 131718 | 224309 | 552137 | 1004774 | 1512705 | 2006827 | 2156867 | 2168540 | 2263738 |
Az adatok rögzítése során a tartály vizuális megfigyelésére nem volt lehetőség.
5. A kísérleti adatok részletes elemzése
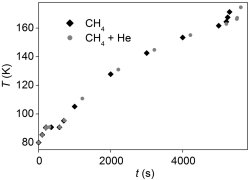
A kísérleti adatok alapján megszerkeszthető két melegedési görbe (vagyis az idő függvényében a hőmérséklet) a 2. ábrán látható. Az x tengely az állandó fűtési sebesség miatt 10-zel való szorzással akár energiává is átalakítható.
Mindkét melegedési görbén két jellegzetes pont azonosítható. Az első ilyen pont az, ahol a hőmérséklet időben állandóvá válik néhány percre (90,67 K az első görbén, 90,74 K a másodikon). Ilyen körülmények között a hőközlés ellenére sem változik a hőmérséklet, márpedig ez csak fázisátmenet következménye lehet: ezen a hőmérsékleten a szilárd állapotban lévő metán megolvad. A másik jellegzetes pont a nagy hőmérsékleten (164,40 K illetve 166,30 K) jelentkező töréspont, amely után a hőmérséklet-növekedés sokkal rohamosabbá válik. Eddig a pontig a tartályban folyékony és gázhalmazállapotú metán is jelen van, utána viszont már csak a gázfázis. Erről úgy is meg lehet győződni, hogy a tökéletes gázok állapotegyenletével kiszámoljuk az adott teljes térfogathoz, nyomáshoz és hőmérséklethez tartozó anyagmennyiséget. Az első kísérlet utolsó pontjára ez a következő:
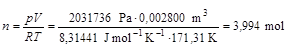
Ez gyakorlatilag megegyezik a metánra a 64,0 g tömegből és 16,04 g/mol moláris tömegből számolható anyagmennyiséggel. Hasonlóan a második kísérlet utolsó pontjából:
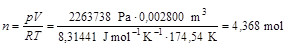
Ez a 64,0 g metán és az 1,471 g hélium összesített anyagmennyiségével egyezik meg.
A töréspontot 164,40 K, illetve 166,30 K hőmérsékleteken az okozza, hogy utána már nincs folyadékfázis. A hőmérséklet-növekedés azért válik sokkal gyorsabbá ezután, mert a folyadék párolgása, amely viszonylag nagy hőt igényel, többé már nem játszódik le, vagyis csak a gáz (illetve a második esetben a gázkeverék) melegszik. A szilárd anyag és a folyadék párolgása folyamatos a kísérlet során, de a folyadék forrása egyik esetben sem következik be, mert ez a jelenség csak nyílt rendszerekben, állandó külső nyomás fenntartása esetén lehetséges. Az első kísérletben a mért nyomásértékek 164,40 K alatt a szilárd vagy folyékony metán gőznyomásával egyenlőek. Az első kísérletben mért olvadáspont és az itt tapasztalt gőznyomás egyúttal a metán hármaspontját is definiálják, vagyis azt az egyedi nyomás- és hőmérsékletértéket, ahol a metán egyszerre három fázisban (szilárd, folyadék és gáz) jelen van egyensúlyban. A metán kritikus pontjának állandói nem becsülhetők meg az adatokból, csak annyi állapítható meg, hogy a kritikus hőmérséklet 164,40 K, a kritikus nyomás 1,95 MPa, a kritikus sűrűség pedig 64,0 g / 2800 cm3 = 0,023 g/cm3-nél nagyobb. Ezek az alsó becslések nem mondanak ellent az irodalmi adatoknak, amelyek szerint a metán kritikus hőmérséklete 190,56 K, kritikus nyomása 4,60 MPa, kritikus sűrűsége pedig 0,16 g/cm3.
A metán az első kísérletben legalább 371, a második kísérletben 372 s-ig olvad, ennek alapján az olvadáshő a gáztérben lévő metán mennyiségének elhanyagolásával a következőképp becsülhető meg:
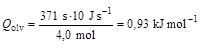
Ez az érték valamivel kisebb lehet, mint a tényleges olvadáshő, mert a számítás az olvadáshoz szükséges hőt alulbecsli (lehet, hogy kicsit hosszabb ideig tartott az olvadás az adatokban állandó hőmérsékletűként jelzett szakasznál), az anyagmennyiséget viszont felülbecsli (nem a metán teljes anyagmennyisége olvad meg, mert egy része gázfázisban van).
A Clausius-Clapeyron-egyenlet egyik alakja szerint egy anyag gőznyomása (
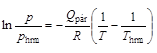
A képletben
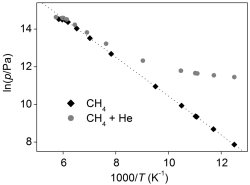
Az első kísérletsor adatai igen jól illeszkednek egy egyenesre abban a tartományban, ahol a mért nyomás valóban egyenlő a gőznyomással (80,00-164,40 K). 164,40 K fölött már nem a metán gőznyomását méri a berendezés, ezért eltérés tapasztalható. A 3. ábrán látható, illesztett egyenes meredeksége -1032 K, így a metán párolgáshője a gázállandóval való szorzás után 8,6 kJ/mol-nak becsülhető. A második kísérletben hasonló következtetéseket nem lehet levonni, mert ott a hélium is befolyásolja a nyomást.
Egy másik fontos következtetést viszont le lehet vonni a hélium jelenlétében mért adatokból. Az első kísérletben olvadás közben a nyomás állandó, hiszen ez egyenlő a metán gőznyomásával az adott hőmérsékleten, függetlenül a gőztér térfogatától. A második esetben a nyomás csekély mértékben növekszik olvadás közben. A metán parciális nyomása itt sem változhat az állandó hőmérséklet miatt, a nyomásnövekedést így a hélium parciális nyomásának a növekedése okozza. Ez viszont állandó hőmérsékleten csak akkor növekedhet, ha a gáztér térfogata csökken. A gáztér térfogata csak úgy csökkenhet, ha a kondenzált fázis térfogata közben növekszik. Ez azt jelenti, hogy a metán olvadás közben kitágul, vagyis a szilárd metán sűrűsége nagyobb, mint a folyékony metáné ugyanolyan hőmérsékleten. A kísérletekből a két sűrűség meg is becsülhető: először a 2. ábrán bemutatott adatokból és a Clausius-Clapeyron-egyenletből kiszámítjuk a metán gőznyomását 90,74 K hőmérsékleten, ez 11805 Pa-nak adódik. A második kísérletben tehát ennyi a metán parciális nyomása olvadás közben. Így a hélium parciális nyomása a folyamat elején 115162 - 11805 = 103357 Pa, a végén pedig 116242 - 11805 = 104437 Pa. A hélium anyagmennyisége a bemért tömegből kiszámolható (1,471 g / 4,003 g/mol = 0,03675 mol): erről feltételezhető, hogy teljes egészében gázfázisban van, mert a hélium kritikus hőmérséklete minden anyag közül a legalacsonyabb (5,2 K), oldhatósága folyékony metánban pedig az amerikai űrkutatási ügynökség, a NASA adatai szerint 90 K hőmérsékleten és 100 000 Pa nyomáson kisebb 0,01 mol%-nál. A tökéletes gázokra vonatkozó állapotegyenlet alapján kiszámolható a gázfázis térfogata:

Ugyanilyen számolás a gázfázis térfogatát az olvadás végén 0,002655 m3-nek adja. A tartály teljes térfogata 2800 cm3, ezért a kondenzált fázis térfogata az olvadás elején 2800 - 2683 = 127 cm3, az olvadás végén pedig 2800 - 2655 = 145 cm3. Az olvadás elején a metán parciális nyomásából és a gázfázis térfogatából a gázhalmazállapotú metán anyagmennyiségére 0,04198 mol számolható, a az olvadás végén ez 0,04154 mol. A szilárd metán sűrűsége tehát:
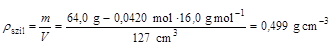
Hasonló számolással a folyékony metán sűrűsége 90,74 K hőmérsékleten:
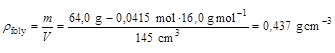
Ugyanezzel a gondolatmenettel a folyékony metán sűrűsége 95,49 K-en 0,370 g/cm3-nek becsülhető. Ilyen típusú számítások az első kísérletsor adatai alapján nem végezhetők, mert ott nem lehetséges a két külön fázisban lévő metán anyagmennyiségét megbecsülni a kísérleti adatokból.
További következtetések vonhatók le abból a tényből, hogy a második kísérletben a hélium jelenléte miatt uralkodó nagyobb nyomás a metán olvadáspontjának csekély mértékű növekedését okozta az első kísérlethez képest. Az ilyen, külső nyomás hatására bekövetkező olvadáspont-növekedést a Clapeyron-egyenlet írja le:
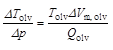
Az egyenletben
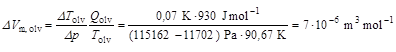
A két fázis már kiszámolt sűrűségéből a szilárd metán móltérfogata 16,0 g/mol / 0,499 g/cm3 = 32,1 cm3/mol, a folyékony metáné 16,0 g/mol / 0,437 g/cm3 = 36,6 cm3/mol. A két érték különbsége 4,5 cm3/mol, amely egy kicsit kisebb, mint az olvadáspont-növekedésből ugyanerre a mennyiségre számolt érték (7 cm3/mol). Az eltérés fő oka az lehet, hogy a Clapeyron-egyenletet csak olyan közelítő formájában lehetett használni, ahol meglehetősen nagy nyomásváltozás szerepel.
6. A balesetre levonható következtetések
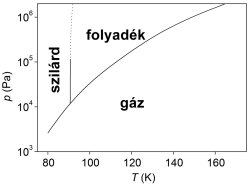
A kísérleti adatok alapján felrajzolható a metán fázisdiagramjának egy része, ez látható a 4. ábrán. A fázisdiagram x tengelyén a hőmérséklet, y tengelyén a nyomás szerepel, s belőle le lehet olvasni azt, hogy meghatározott körülmények között melyik fázis a stabil. 4. ábra A metán fázisdiagramjának egy részlete
A fázisdiagram alapján a következő megállapításokat lehet tenni:
- A Pirx kapitány által mért nyomáson és hőmérsékleten (128 K és 154 kPa) a metán gázfázisban stabil. Így ha korábban volt is tó a helyen, az a kapitány odaérkezéséig elpárologhatott.
- A szonda adataiból kinyert nyomáson és hőmérsékleten (94 K és 142 kPa, bár ezek helyessége később kifejtett okok miatt kétségbe vonható) a metán folyékony állapotban stabil. Ilyen körülmények között lehetett metántó a szonda leszállási helyén. Szilárd metán ekkor nem létezhetett egyensúlyban. Azonban ismert az a jelenség, hogy a földi tengerekben hosszú ideig előfordulnak úszó jéghegyek fagypont fölötti hőmérsékleteken is. A baleset idejében a Titánon a hőmérséklet kb. 3 K-nel volt csak magasabb, mint a metán olvadáspontja. Ezért nem lehetetlen, hogy még olvadófélben lévő metánjég is volt a tóban. Ennnek valószínűsége azonban nem nagy, mert a szilárd metán olvadáshője elég kicsi, tehát a nem egyensúlyi állapot csak rövid ideig állhat fenn.
- A folyékony metán sűrűsége 94 K-en kisebb, mint 90,67 K-en (0,437 g/cm3), de nagyobb, mint 95,49 K-en (0,370 g/cm3). Az űrszonda átlagos sűrűsége 0,34 g/cm3, ezért valóban úszhatott a metántóban.
- Mind a szilárd metán, mind a vízjég sűrűsége nagyobb, mint a folyékony metáné, ezért metánból vagy vízből álló jégtönb semmiképpen nem úszhat egy metántó felszínén.
A Titán szirénjei által adott magyarázat tehát nem hiteles. Valószínű, hogy a szondát a leszállást követően kaontorpedóval elpusztították, s utána találták ki a történetet a jégheggyel való ütközésről, amelyet arra alapoztak, hogy az emberek számára egy folyadékban úszó jéghegy látványa szokásosnak számít. Ezt a jég azon anomális tulajdonsága okozza, hogy olvadáskor csökken a térfogata. A Titán szirénjei bizonyíthatóan tudnak a víz ezen sajátságáról, mert a közelmúltban a Földkultúra-terjesztési program keretében az 1997-ben készült, Oscar-díjas, Titanic című filmet is megkapták számukra érthetővé tett formában.
Végül azt is észrevételezni kell, hogy a szondából kinyert hőmérsékleti és nyomásadatok kétségbe vonhatakó. A Pirx kapitány által feljegyzett értékek egyértelműen nyári évszakra utalnak, míg a szondából kinyert adatok télre. Egy égitesten az évszakok váltakozását a Naphoz viszonyított helyzet határozza meg. A Titán a Szaturnusszal együtt mozog a Nap körül, a keringés idő 29,4 év. Ezért a Titánon az időjárás nem fordulhat néhány hónap alatt téliből nyáriba. Könnyen elképzelhető, hogy a Titán szirénjei - a kitalált történetük alátámasztására - ezeket az adatokat meghamisították az alatt a néhány hónap alatt, amíg a szondához háborítatlanul hozzáfértek. Ezt a feltételezést támasztja alá az a tény is, hogy Pirx kapitányt nem érte támadás a Titán felszínén, noha öt és fél percnél jóval hosszabb ideig tartózkodott ott.
![]() 2012.12.13.
2012.12.13.
