ScienceBits
Lente Gábor blogja
Mengyelejev tévedései
KÖZÉPISKOLAI KÉMIAI LAPOK, SZAKMAI

Dimitrij Ivanovics Mengyelejevet (1834-1907) a periódusos rendszer atyjaként tiszteli a tudománytörténet. Habár már korábban is sokan foglalkoztak az elemek rendszerezésével, pl. Alexandre Emile Béguyer De Chancourtois (1820-1886), John Newlands (1837-1898), William Odling (1829-1921), Gustavus Hinrichs (1836-1923) és Julius Lothar Meyer (1830-1895), az orosz tudós munkásságának két fontos vonás adott kiemelkedő jelentőséget. Egyrészt Mengyelejev élete végéig fáradhatatlanul népszerűsítette szakmai körökben a periódusos rendszert és a mögötte rejlő periódusos törvényt. Másrészt részletes jóslatokat fogalmazott meg a törvényből szükségszerűen következő, de még fel nem fedezett elemek létezésére, tulajdonságaira, és a természetben való keresésükhöz is útmutatót adott.
Mengyelejev a szibériai Tobolszk városában született legfiatalabbként egy tizennégy gyermekes családban. Édesapja korán meghalt, édesanyja viszont igen sok időt és energiát szentelt Dimitrij természettudományos oktatásának, aki egyetemei évei alatt Robert Bunsen (1811-1899) laboratóriumában dolgozott Heidelbergben, s 1865-ben hazájában szerzett doktori fokozatot. Periódusos rendszerét 1869-ben alkotta meg, miközben egy kémiai tankönyv („Основы Химии” = A kémia alapjai) írásán dolgozott és azon töprengett, hogyan is lehetne az elemeket valamiféle logikus sorrendben bemutatni. Hamar rájött arra, hogy ezek az eredmények nemcsak oktatási, hanem tudományos szempontból is érdekesek lehetnek, ezért folyóiratcikk formájában is publikálta őket előbb oroszul, majd a kor legfontosabb tudományos nyelvén, németül is. Az 1869-ben németül publikált első periódusos rendszert mutatja be az 1. ábra. Ezt a formát manapság rövid periódusos rendszerként említik és viszonylag ritkán használják. A ma leginkább használt, nyújtott formát Mengyelejev nem kedvelte különösebben, s az csak jóval később, Alfred Werner (1866-1919) Nobel-díjas tudós hatására terjedt el.
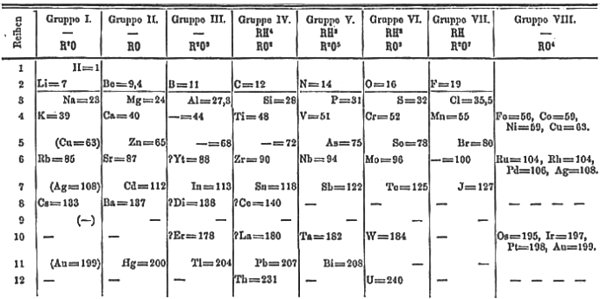
Az első bekezdésben már szó volt arról, hogy Mengyelejev hírnevét elsősorban a jóslatok alapozták meg. Ezen jóslatok egy része már az 1. ábrából is kiolvasható. Az rendszer elsődleges rendezőelve az atomtömegek sorrendje, ezen logika szerint a bór alatt addig még nem ismert elemnek kellett lennie („- = 44”). Mai szemmel nézve kicsit talán zavaró, hogy jobbra igazítva a bór és ezen megjósolt elem között még az alumínium is ott van az 1. ábrán, és első nézésre az is furcsaság lehet, hogy a periódusos rendszer modern formájában a bór alatt éppen az alumínium van. Ennek a hiányzó elemnek Mengyelejev ideiglenesen az ekabór (= bór alatti elem) nevet adta, és a körülötte lévő elemek tulajdonságainak felhasználásával meg is jósolta néhány jellemzőjét. Ugyanez történt az alumínium alatti (ekaalumínium) és a szilícium alatti (ekaszilícium) elemmel. Elég jelentős magabiztosság és intuíció kellett ahhoz, hogy két, közvetlenül egymás után következő elem hiányát jósolja meg a tudós egy olyan táblázatban, ahol az elemek túlnyomó többségét már ismertnek gondolta. A nem sokkal későbbi felfedezések azonban fényesen igazolták Mengyelejev jóslatait. Az ekaalumíniumot a francia Emile Lecoq De Boisbaudran (1838-1912) 1875-ben fedezte fel és galliumnak nevezte el. Az ekabórra is csak 1879-ig kellett várni, a felfedező a svéd Lars Fredrik Nilson (1840-1899) volt, aki a szkandium nevet választotta. Az ekaszilíciumot 1886-ban a német Clemens Winkler (1838-1904) azonosította, és germániumnak keresztelte. Tehát két évtizeden belül, Mengyelejev munkájától függetlenül kísérletileg igazolták ezeket a jóslatokat.
Mengyelejev intuíciója más területen is igen jól működött. A berillium és urán esetében például azt feltételezte, hogy ezen elemek általánosan elfogadott vegyértéke, és ebből következően atomtömege is hibás. Új vegyértékeket feltételezve jutott a berillium 9,4-es és az urán 240-es atomtömegéhez, ami lényegében a ma ismert értékek közelítése akkori pontossággal.
Mai ismereteink szerint az atomtömegek monoton növekedése három helyen is megtörik a periódusos rendszerben. A legkisebb törés a kobalt és nikkel között van (Co: 58,93 és Ni: 58,70). Ezen elemek az 1. ábrán lévő rendszerben azonos értékkel (59) szerepelnek, de sorrendjüket a kémiai sajátságok alapján jól sejtette meg Mengyelejev. Nagyobb a különbség a tellúr és a jód között (Te: 127,6 és I: 126,9). Az 1. ábra itt is a helyes sorrendet mutatja, azonban ebben az esetben Mengyelejev elkövetett egy kegyes csalást: azt feltételezte, hogy a tellúr atomtömegét hibásan határozták meg kísérletileg, s a valós értéknek kicsit kisebbnek kell lennie. A legnagyobb ilyen anomália az argon és a kálium között van (Ar: 39,95 és K: 39,10). Ez persze Mengyelejev számára a legkevésbé sem jelentett gondot, mert az argont nem ismerte, azt csak a XIX. század legvégén fedezték fel. A nemesgázok létezését Mengyelejev nem láthatta előre, hiszen 1869-ben még egyetlen elemet sem ismertek ebből csoportból. Azt se felejtsük el, hogy a rendszám fogalma ekkor még ismeretlen volt, s csak 1913-ban alkották meg az anyagok röntgensugárzással való kölcsönhatását leíró Moseley-törvény révén. Azonban Mengyelejev rendszerében a halogének és alkálifémek között volt hely egy új oszlopnak! Így a nemesgázok beillesztése az 1890-es években nem okozott lényeges problémát.
Mengyelejev utolsó, 1904-ben összeállított periódusos rendszerét mutatja be a 2. ábra. Ebben már szerepelnek a nemesgázok és az addigra felfedezett, 1869-ben megjósolt elemek is. A nagy tudós az atomtömegek sorrendjéhez láthatóan szenvedélyesen ragaszkodott: az argont helyes atomtömegénél kisebb, 38-as értékkel vette fel a rendszerbe, s a tellúr esetében 35 év alatt is csak annyi engedményre volt hajlandó, hogy a jóddal azonos atomtömeget tulajdonított neki. Az évek során Mengyelejev kezdeti sikerén felbuzdulva további jóslatokat is tett. Ekamangán (az 1. ábrában „- = 100”) és trimangán néven például a XX. század elején még nem ismert, mangán alatt lévő, később technéciumnak és réniumnak elnevezett elemek létezését jelezte előre. Ugyancsak sikeres volt a dvitellúr (polónium), a dvicézium (francium) és az ekatantál (protaktínium) jóslata.
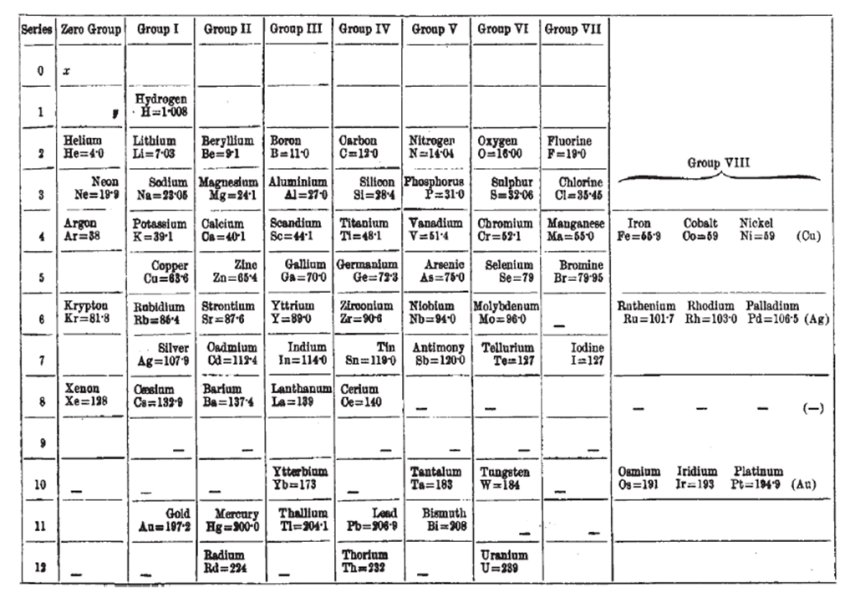
A 2. ábrát alaposan áttanulmányozva viszont azt láthatjuk, hogy abban bizony két, a hidrogénnél könnyebb elem is található, amelyet x és y jelöl. Mengyelejev jóslatában mindkettőt a nemesgázok oszlopába, a hélium fölé helyezte. Az x elemet a fizikusok által akkor létezőnek gondolt éter megfelelőjének hitte, az y jelölésű elemet pedig több néven is említette munkáiban, ezek közül a leggyakoribb a korónium volt. 1904-ben még alig egy évtized telt el az első nemesgáz felfedezése óta, ezért Mengyelejev joggal gondolhatta, hogy lehet még addig ismeretlen közöttük, amely esetleg a Földön nem is fordul elő. Ezen kívül egy sokkal filozofikusabb jellegű oka is volt az x és y feltételezésre. Akkoriban sokan elfogadtak egy Prout-hipotézis nevű elméletet, amely azt mondta ki, hogy minden egyes atom valamilyen módon végső soron hidrogénatomokból áll. Ebből persze az következett, hogy nem lehetséges a hidrogénnél könnyebb atomot elképzelni. Mengyelejev viszont ádáz ellensége volt ennek a feltételezésnek. Nagyon jól tudta, hogy az atomtömegek nem mindig egész számú többszörösei a hidrogén atomtömegének (az 1. ábrán a berillium, alumínium vagy klór atomtömege a példa erre), bár az izotópok létezéséről természetesen sejtése sem lehetett még abban az időben. A Prout-hipotézissel szembeni ellenérzését azzal is kinyilvánította, hogy az x és y elemek jóslataihoz élete végéig ragaszkodott annak ellenére is, hogy semmilyen kísérleti adat nem utalt azok létezésére.
Az 1. táblázat bemutatja az összes Mengyelejev által megjósolt elemet. Az éter és a korónium atomtömegét az ismert nemesgázoknál tapasztalható tendenciák alapján becsülte meg. A táblázatból az is látható, hogy nemcsak x és y volt téves elemjóslat Mengyelejev életében. A további hibás jóslatok (ekacérium, ekamolibdén, ekanióbium, ekakadmium, ekajód és ekacézium) mind azzal kapcsolatosak, hogy a lantanidák csoportjának tagjait ugyan nagyrészt még Mengyelejev életében megismerték, de megfelelő elhelyezést számukra a periódusos rendszerben sokáig nem találtak. Ugyanilyen probléma az aktinidákkal egyáltalán nem volt, ezeket nagyrészt csak 1940 után fedezték fel. A periódusos rendszerben még 1944-ben is a tóriumot a hafnium, az uránt pedig a volfrám alá írták.
| Mengyelejev által megjósolt és ténylegesen felfedezett elemek | ||||
|---|---|---|---|---|
| feltételezett elem | feltételezett atomtömeg | tényleges elem | felfedezés éve | tényleges atomtömeg |
| éter | 0,17 | ─ | ||
| korónium | 0,4 | ─ | ||
| ekabór | 44 | szkandium | 1879 | 44,96 |
| ekacérium | 54 | ─ | ||
| ekaalumínium | 68 | gallium | 1875 | 69,72 |
| ekaszilícium | 72 | germánium | 1886 | 72,61 |
| ekamangán | 100 | technécium | 1939 | 98 |
| ekamolibdén | 140 | ─ | ||
| ekanióbium | 146 | ─ | ||
| ekakadmium | 155 | ─ | ||
| ekajód | 170 | ─ | ||
| ekacézium | 175 | ─ | ||
| trimangán | 190 | rénium | 1925 | 186,2 |
| dvitellúr | 212 | polónium | 1898 | 209 |
| dvicézium | 220 | francium | 1939 | 223 |
| ekatantál | 235 | protaktínium | 1917 | 231,0 |
Összességében a 2. táblázat azt a meglepő dolgot mutatja, hogy a Mengyelejev által megjósolt elemeknek csak fele létezett a valóságban. Hogyan fordulhatott elő vajon, hogy míg a sikeres jóslatok jelentős érvek voltak a periódusos törvény érvényessége mellett, addig a sikertelenek nem váltak a tudományos elfogadás gátjaivá? Erre a kérdésre nehéz válaszolni. Érdemes megjegyezni, hogy a sikertelen jóslatok sem voltak logikátlanok a periódusos rendszerben a tudomány akkori állása szerint. Pusztán annyi történt, hogy később másféle gondolatmenetek érvényességét igazolta a kémia. Ne felejtsük el, hogy Mengyelejev sem a rendszám fogalmát, sem az atomok elektronszerkezetét nem ismerhette: manapság ezek teszik a periódusos rendszer felépítésének elvét egyértelművé.
Senki sem tévedhetetlen, Mengyelejev sem volt az. Az ő tévedéseit azonban a tudomány készségesen megbocsátotta, sőt talán el is felejtette, mert munkájának hozzájárulása a kémia fejlődéséhez felmérhetetlenül nagy volt. Az összes tudós közül talán ő szolgát rá a leginkább, hogy elemet nevezzenek el róla. Ezt mutatja az a tény is, hogy a 101-es elem számára a mendelévium nevet nem az orosz tudós honfitársai, hanem egy amerikai kutatócsoport javasolta.
![]() 2009.09.26.
2009.09.26.
